電解飽和食鹽水總方程式:2NaCl+2H2O=通電=2NaOH+H2↑+Cl2↑。電解飽和食鹽水后,食鹽水中的氯化(NaCl)與水(H2O)發生電離,分別在陰極與陽極生成氫氣(H2)與氯氣(Cl2),剩下的氫氧根離子與鈉離子結合生成氫氧化鈉(NaOH),工業上常用電解食鹽水制取氫氧化鈉。

電解飽和食鹽水總方程式:2NaCl+2H2O=通電=2NaOH+H2↑+Cl2↑
電解飽和食鹽水后,食鹽水中的氯化(NaCl)與水(H2O)發生電離,分別在陰極與陽極生成氫氣(H2)與氯氣(Cl2),剩下的氫氧根離子與鈉離子結合生成氫氧化鈉(NaOH),工業上常用電解食鹽水制取氫氧化鈉,由于氯離子或氯氣與氫氧化鈉溶液接觸會生成氯化鈉和次氯酸鈉(NaClO)。
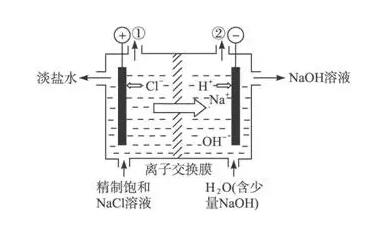
電解飽和食鹽水電極反應方程式:
陽極:2Cl--2e-=Cl2↑(2個氯離子失去2個電子,陽極發生氧化反應)。
陰極:2H++2e-=H2↑(2個氫離子得到2個電子,陰極發生還原反應)。
為了和化學方程式一致,陰極其實寫成下式更好,因為氫離子來自水,水在離子方程式不拆:陰極2H2O+2e→H2↑+2OH-。電解總反應:2NaCl+2H2O=電解=H2↑+Cl2↑+2NaOH(陰極產生H2、NaOH,陽極產生Cl2)。

粗鹽提純基本步驟:溶解、過濾、蒸發結晶。經過這幾步操作后除去的是不溶性雜質。具體步驟:準備器材:托盤天平,量筒,燒杯,玻璃棒,藥匙,漏斗,鐵...

加熱氯酸鉀的化學方程式為:2KClO?=2KCl+O?↑,MnO?寫在等于號的上面,加熱符號(Δ)寫在等于號下面。氯酸鉀加熱時不用放棉花,放...

復分解反應的定義:復分解反應是兩種化合物之間的組分交換,產生另外兩種化合物的反應,它的本質是水溶液中兩種具有復分解交換離子的化合物,結合形成...

過濾后濾液仍然渾濁有三種可能原因:沉淀顆粒太小。如膠體類沉淀,顆粒太小,可以透過濾紙,尤其是普通的定性濾紙。形成的是乳濁液而不是固液混合物(...

實驗室制取氧氣的三個化學方程式:加熱氯酸鉀和二氧化錳2KClO3==2KCl+3O2↑(條件:MnO2、加熱);加熱高錳酸鉀2KMnO4==...

一氧化氮沒有顏色。一氧化氮為氮氧化合物,化學式是NO,相對分子質量30.01,氮的化合價為+2。是一種無色無味氣體難溶于水的有毒氣體。由于一...

地殼中含量居前五位的元素為氧、硅、鋁、鐵和鈣。在地殼中最多的化學元素是氧,它占總重量的48.6%,其次是硅,占26.3%。鋁、鐵、鈣、鈉、鉀...

硫酸鈉溶解度:溫度100℃時溶解度42.5。硫酸鈉是硫酸根與鈉離子化合生成的鹽,硫酸鈉溶于水,其溶液大多為中性,溶水時為堿性,溶于甘油而不溶...